- Главная
- Для учителя
- Архив заданий олимпиад по физике за 2009-2015 годы
- Владимир Анатольевич Зверев предлагает
- Несколько ссылок на работы Анатолия Шперха
- Общие вопросы методики обучения физике
- Статьи Александра Борисовича Рыбакова
- Важнейший общефизический принцип остается непонятым
- Рыбаков А. Б. Почитаем «Физику» вместе
- Рыбаков А.Б. Несколько замечаний о «Физике (ПС)», №10, 2015
- Рыбаков А.Б. О №12 «Физики (ПС)» и динамике автомобиля, или Спасут ли школу вузовские преподаватели?
- А.Б.Рыбаков Банджи-джампинг, сохранение импульса и уравнение Мещерского
- Рыбаков А.Б. О вращении Земли и всяком таком, или Удивительная физика в журнале «Физика (ПС)», №2/2015
- Экзамены
- Конспекты
- История физики
- Хронология физики
- Физики. Краткие биографии
- Дополнения к биографиям
- Нобелевские премии по физике
- История методики обучения физике
- Календарь на текущий год
- Физический календарь на 2026 год
- Физический календарь на 2025 год
- Календарь памятных дат в физике на 2023 год
- Юбилейные и памятные даты из истории физики в 2022 году
- Физический календарь на 2015 год
- Физический календарь на 2016 год. ч. 1
- Физический календарь на 2016 год. ч. 2
- Календарь памятных дат в физике на 2019 год
- Физики в Петербурге-Петрограде-Ленинграде
- Библиотека
- Медиатека
- О нас
Радиоактивность. Строение атома.
|
Радиоактивность |
|
|
1896 г. Французский физик А. Беккерель, изучая явление люминесценции солей урана, установил, что урановая соль испускает лучи неизвестного типа, которые проходят через бумагу, дерево, тонкие металлические пластины, ионизируют воздух. |
|
|
1897-98 г. Мария Склодовская-Кюри и Пьер Кюри, исследуя урановые руды, обнаружила новые химические элементы: полоний, радий. Явление самопроизвольного превращения неустойчивых изотопов в устойчивые, сопровождающееся испусканием частиц и излучением энергии, называется естественной радиоактивностью. Все химические элементы, начиная с порядкового номера 83, являются радиоактивными. |
|
|
Виды радиоактивных излучений |
|
|
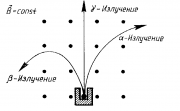
1898 г. подвергая радиоактивное излучение действию магнитного поля, Э. Резерфорд выделил два вида лучей: α-лучи — тяжелые положительно заряженные частицы (ядра атомов гелия) и β-лучи — легкие отрицательно заряженные частицы (тождественны электронам). |
|
|
В 1900 г. П. Виллард открыл гамма-лучи — нейтральное излучение, где масса покоя равна нулю (аналогично свойствам света, но |
|
|
Гипотеза о том, что все вещества состоят из большого числа атомов, зародилась свыше двух тысячелетий тому назад. Сторонники атомистической теории (Демокрит, Левкипп, Анаксагор, Анаксимандр, Эпикур, Лукреций Кар) рассматривали атом как мельчайшую неделимую частицу и считали, что все многообразие мира есть не что иное, как сочетание неизменных частиц — атомов. Демокрит: существует предел деления атома. Аристотель: делимость вещества бесконечна. Париж, 1626 г.: учение об атоме запрещено под страхом смерти. Сторонниками атомистической теории были М.В. Ломоносов, Ж. Гей-Люссак, Д. Дальтон и др. |
|
|
Толчком к подробному изучению строения атома послужили: - открытие рентгеновского излучения (1895 г., В.К. Рентген); - открытие радиоактивности и новых радиоактивных элементов (1896 г., А. Беккерель, М. и П. Кюри); - открытие электрона (1896 г., Дж. Дж. Томсон). |
|
|
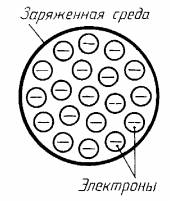
Мысль об электронном строении атома, впервые высказанную В. Вебером в 1896 г., развил X. Лоренц: электроны входят в состав атома. Опираясь на эти открытия, Дж. Томсон в 1898 г. предложил модель атома в виде положительно заряженного шара радиусом 10-10 м. в котором плавают электроны, нейтрализующие положительный заряд. |
|
|
Ядерная модель атома |
|
|
Экспериментальная проверка модели Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом. Идея опыта заключалась в изучении рассеяния α-частиц (заряд +2е, масса 6,64.10-27 кг) на атомах. α-частицы были выбраны, т.к. их кинетическая энергия много больше кинетической энергии электронов (β-лучи) и, в отличие от γ-лучей они имеют электрический заряд. |
|
|
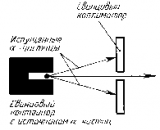
Пучок α-частиц пропускался через тонкую золотую фольгу. Золото было выбрано как очень пластичный материал, из которого можно получить фольгу толщиной практически в один атомный слой. Опыты были повторены и на других материалах |
|
|
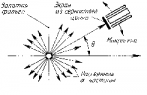
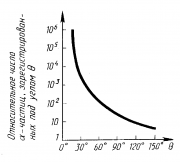
Э. Резерфорд и его помощники Г. Гейгер и Э. Марсден обнаружили, что какая-то частьa-частиц отклоняется на довольно значительный угол от своего первоначального направления, а небольшая часть отражается от фольги. Но согласно модели атома Томсона эти a-частицы при взаимодействии с атомами фольги отклоняются на малые углы, порядка 2°. Резерфорд показал, что модель Томсона находится в противоречии с его опытами. Обобщая результаты своих опытов, Резерфорд предложил ядерную (планетарную) модель строения атома:
|
|
|
Расчеты показали, что a-частицы, которые взаимодействуют с электронами в веществе, почти не отклоняются. Только некоторые a-частицы проходят вблизи ядра и испытывают резкие отклонения. Если между зарядами действует кулоновская сила При расчете учитывают, что |
|
|
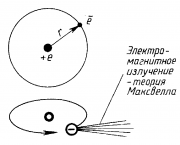
Однако предложенная модель строения атома не позволила объяснить устойчивость атома: - ускоренное движение электрона согласно теории Максвелла сопровождается электромагнитным излучением, поэтому энергия электрона уменьшается, и он движется по спирали, приближаясь к ядру. Казалось бы, электрон должен упасть на ядро (расчет показывает, что это должно произойти за 10-8 с), так как при движении по спирали уменьшается энергия электрона, в действительности атомы являются устойчивыми системами; - спектр излучения при этом должен быть непрерывным (должны присутствовать все длины волн). На опыте спектр получается линейчатым; - нет ответа на вопрос о строении ядра. Если в него входят только положительные частицы, то почему они не отталкиваются? |
|